近日,我校化学化工学院王斌教授课题组在化学领域权威期刊《美国化学会志》发表题为“Catalytic Asymmetric cis-Dihydroxylation of Quinones Enabled by a Functional Mimic of Rieske Dioxygenases”的研究论文(J. Am. Chem. Soc. 2026, https://doi.org/10.1021/jacs.5c20048)。该研究模仿自然界金属酶的催化机制,首次实现了非血红素锰配合物催化醌类化合物的不对称顺式双羟化反应,为手性邻二醇类化合物的高效合成提供了绿色新策略。

科学背景:重要的合成难题
手性顺式-1,2-二醇是一类重要的化学结构单元,广泛存在于具有抗肿瘤、抗菌等生物活性的Ⅱ型聚酮天然产物和药物分子中(图1A)。不对称顺式双羟化反应虽是合成该类结构最直接的途径(图1B),但对醌类化合物长期难以奏效。传统Sharpless不对称双羟化等方法面临四大瓶颈(图1C):醌类底物电子缺乏导致C=C双键反应活性低;平面结构对称性强,阻碍手性催化剂有效识别;生成的顺式-1,2-二醇易发生差向异构化;产物对逆羟醛裂解敏感。这一挑战制约了相关天然产物和药物的合成研究。
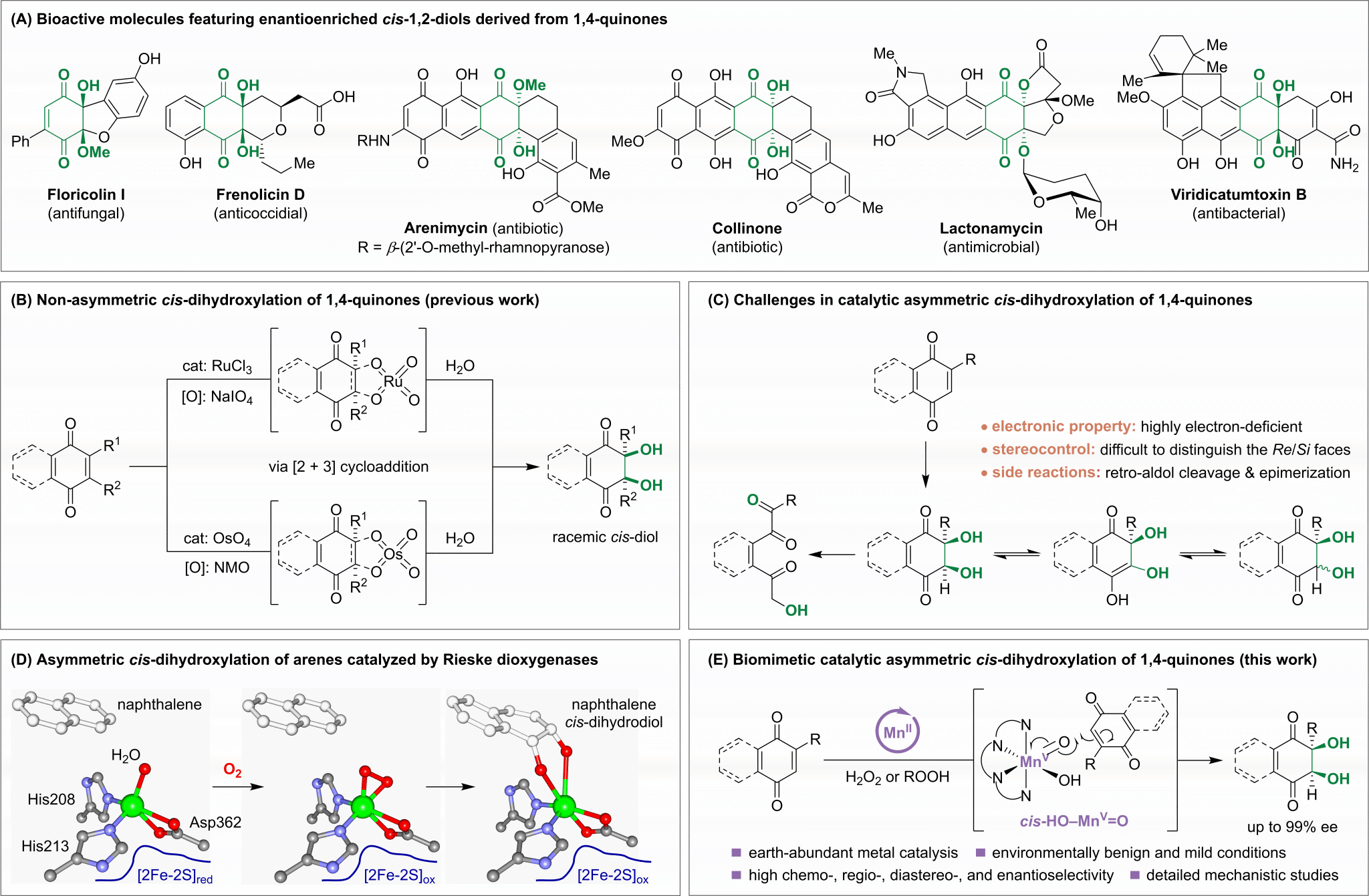
图1. 研究背景及工作设想(图片来源:J. Am. Chem. Soc.)
仿生思路:向大自然寻找答案
我校王斌课题组长期致力于仿生催化研究——一门融合化学与生物学的交叉学科,旨在分子水平上模拟金属酶的催化功能。团队聚焦仿生催化氧化领域,围绕绿色催化与精准合成的核心科学问题,在仿生催化烯烃不对称双羟化与仿生催化C(sp3)−H氧化活化两个方向取得了系统性的研究成果(J. Am. Chem. Soc. 2025,147, 11432;J. Am. Chem. Soc. 2023, 145, 27626; J. Am. Chem. Soc. 2023, 145, 5456; CCS Chem. 2022, 4, 2369; ACS Catal. 2022, 12, 6756)。
受自然界Rieske双加氧酶的启发(图1D),研究团队设计了一种仿生非血红素锰配合物催化剂,以绿色环保的双氧水(H2O2)或烷基过氧化氢为氧化剂,成功实现了醌类化合物的不对称顺式双羟化反应(图1E)。该体系在温和条件下表现出优异的化学选择性、区域选择性和对映选择性(高达99% ee),且完全非对映选择性控制。值得一提的是,这是首次将烷基过氧化氢用作顺式双羟化反应的氧化剂,拓展了氧化剂的选择范围。
机理突破:揭示催化奥秘
研究进一步揭示了反应机理:无论使用何种氧化剂,高亲电性的HO−MnV=O均是关键的活性顺式双羟化中间体(图1E),其生成路径随氧化剂不同而有所差异。这一发现深化了对仿生催化体系的理解,为传统Os、Ru等重金属试剂提供了实用且绿色的替代方案。
该研究得到了国家自然科学基金和山东省高层次人才计划等项目的资助。论文第一作者为我校化学化工学院在读博士研究生郑世鑫。
撰稿:勾志明、丁泽宁 编辑:刘孟頔 编审:张伟